Visaptverošas genoma profilēšanas pakalpojums ļaundabīgiem hematoloģiskiem audzējiem un sarkomām; lai precizētu diagnozi, prognozes un ārstēšanas izvēli un personalizētu pacientu ārstēšanas plānus.1–3



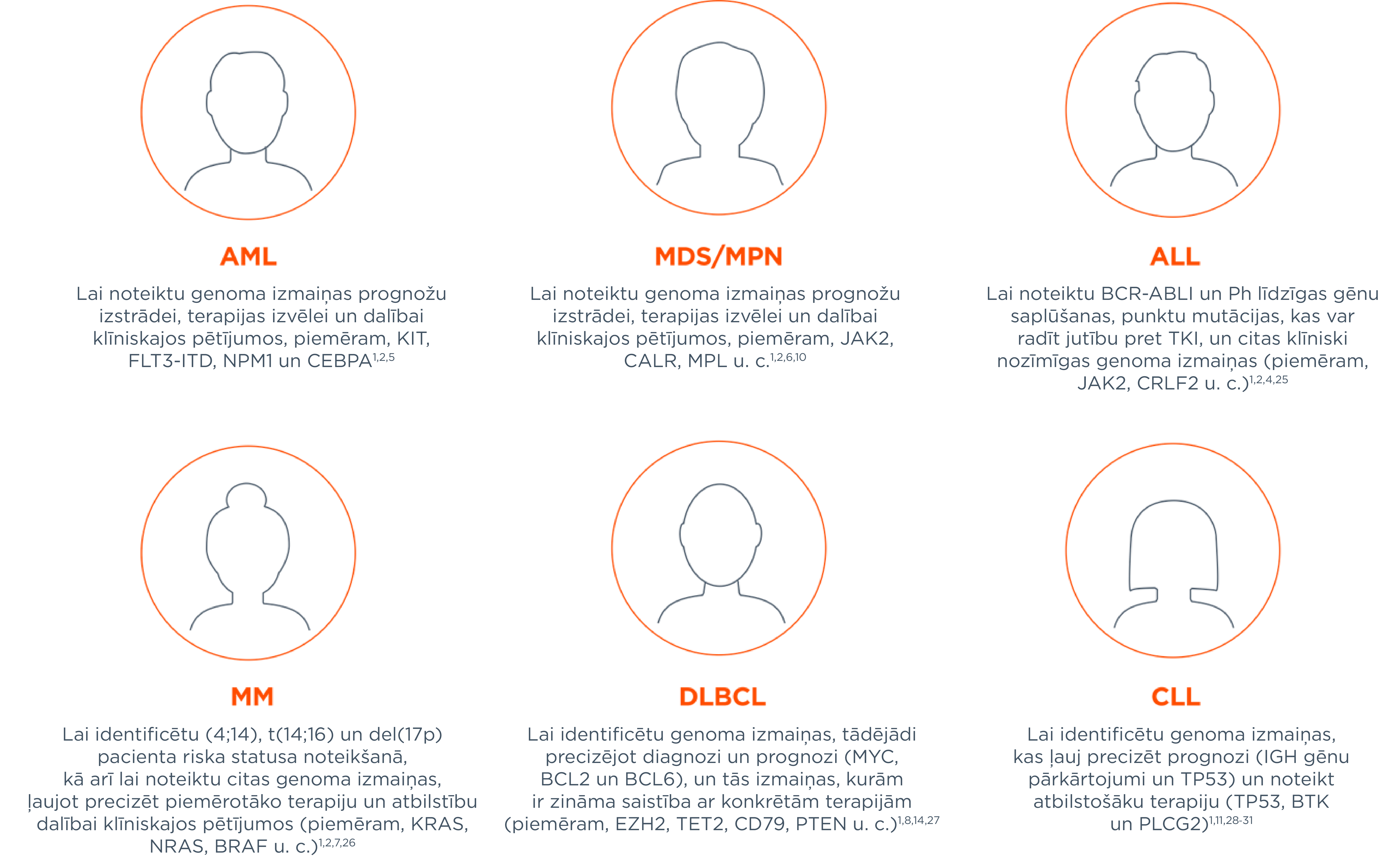
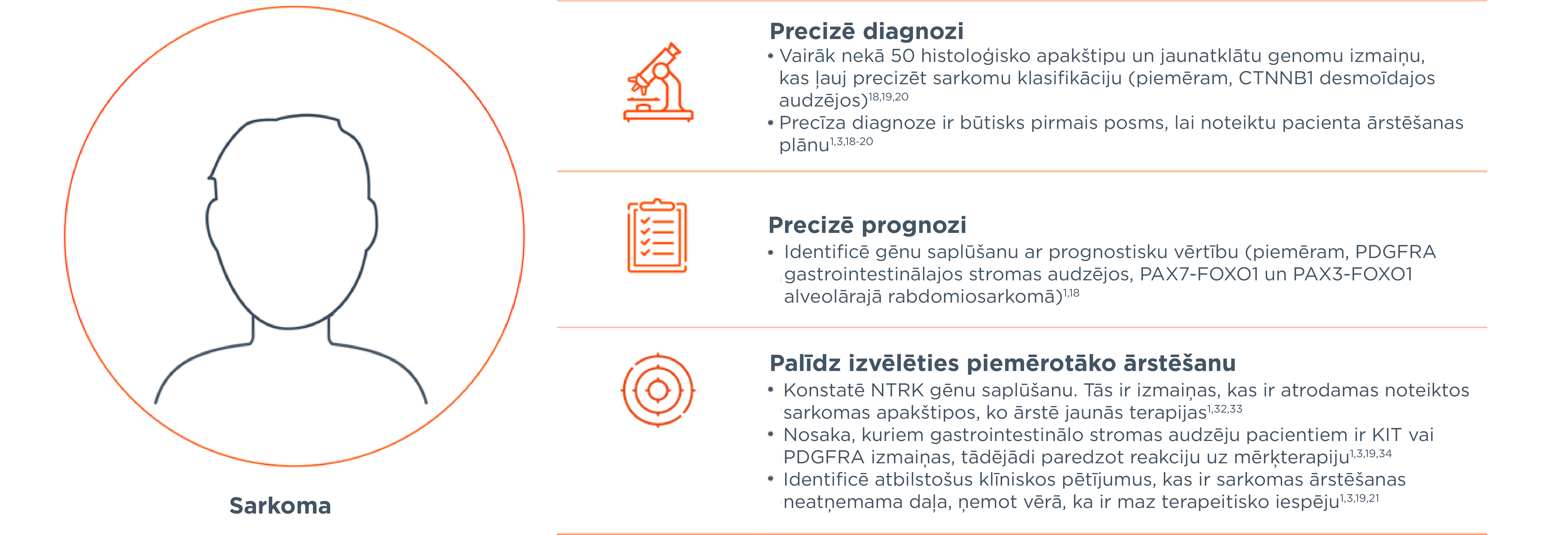
Baudiet priekšrocības, ko sniedz FoundationOne Heme testi, lai precizētu diagnozi, prognozi un piemērotāko ārstēšanu, kā arī lai personalizētu pacientu ārstēšanas plānus.1–3
FoundationOne Heme paraugus var nosūtīt uz mūsu laboratorijām Pencbergā (Penzberg), Vācijā, vai Kembridžā, ASV (attiecīgi pacientiem ES vai no pārējām pasaules valstīm), ļaujot lielākam skaitam pacientu baudīt visaptverošas genoma profilēšanas iespējas, ko sniedz FoundationOne Heme.†
Pieņemamie paraugu veidi:
* Bāzu substitūcijas, insercijas vai delēcijas, kopiju skaita izmaiņas un gēnu pārkārtojumi.
† Lai iegūtu iespējami precīzus rezultātus, venozo asiņu stobriņus vai kaulu smadzeņu aspirātu laboratorijā ir jāsaņem nākamajā dienā pēc parauga savākšanas, jo mutāciju noteikšanas jutība laika gaitā var pasliktināties. Par paraugiem, kas ir saņemti vēlāk, tiek izstrādāts “kvalificētais” ziņojums (qualified report). Pieņem arī FFPE stikliņus
AML, akūta mieloīda leikēmija. ALL, akūta limfoblastu leikēmija. CLL, hroniska limfocitārā leikēmija. GIST, kuņģa un zarnu trakta stromas audzējs. DLBCL, difūza lielo B šūnu limfoma. FFPE, formalīnā nostiprināts un parafīnā ieguldīts. MDS, mielodisplastiskais sindroms. MM, multiplā mieloma. MPN, mieloproliferatīvi jaunveidojumi. MSI, mikrosatelītu nestabilitāte. RMS, rabdomiosarkoma. TKI, tirozīnkināzes inhibitors. TMB, audzēja mutāciju slogs.